CMV R-gene®
Zestaw Real-time PCR do detekcji i pomiaru ilościowego DNA cytomegalowirusa (CMV)
- Dokładny pomiar ilościowy miana wirusa CMV z szerokim zakresem liniowości
- Gotowy do użycia zestaw z kontrolą wewnętrzną i kontrolami ilościowymi w zestawie
- Test posiada certyfikat CE- IVD dla najpopularniejszych systemów do ekstrakcji, platformach real-time PCR oraz różnych typów próbek
Potrzebujesz więcej informacji
CMV R-gene® zalety
Cytomegalovirus (CMV) może powodować poważne powikłania u pacjentów z obniżoną odpornością. Jest to powód, dlaczego potrzebna jest zoptymalizowana detekcja i monitorowanie infekcji wirusem CMV. Test CMV-R-gene® jest doskonałym rozwiązaniem zapewniającym szybką i specyficzną detekcję.
Możliwość wykrycia zakażenia przed objawami klinicznymi poprawia możliwości zarządzania, badania pacjentów podczas leczenia w celu sprawdzenia jego skuteczności i badania po leczeniu w celu monitorowania nawrotów. Dodatkowo – dla zwiększenia efektywności i kompleksowości – używanie wielu zestawów R-gene® pozwala na wykrywanie różnych wirusów z jednej próbki i analizy różnych próbek dla jednego wirusa w tym samym czasie.
- Czułość i powtarzalność
- Dokładny pomiar miana wirusa CMV
- Szeroki zakres liniowości
- Standaryzacja
- Wspólna procedura postępowania z pozostałymi testami R-gene® (EBV R-gene®, HSV1 HSV2 VZV R-gene®, CMV HHV6,7,8 R-gene®, BK Virus R-gene®, Adenovirus R-gene®, Parvovirus B19 R-gene®)
- Taka sama procedura amplifikacji w całej serii produktów pozwala na wykrywanie wielu wirusów jednocześnie
- Protokół do konwersji ilościowych wyników na IU/ml z próbek krwi z wykorzystaniem Pierwszego Międzynarodowego standardu WHO (WHO 1st International Standard)
- Elastyczność
- Zwalidowany dla wielu różnych typów próbek
- Możliwość wykonania manualnej lub automatycznej izolacji próbki z wykorzystaniem takich aparatów jak NucliSENS® easyMAG® oraz przygotowanie reakcji z wykorztaniem takiego systemu jak stacja pipetująca easySTREAM™
- Zatwierdzony dla najpopularniejszych platform real-time PCR
- Zwalidowany dla wielu różnych typów próbek
Wszystko co potrzebne w jednym zestawie
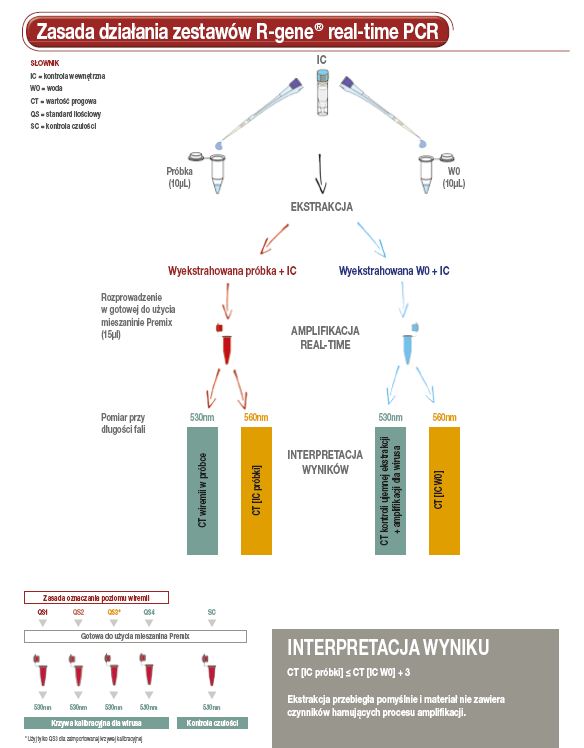
Zestaw CMV R-gene® jest gotowym do użycia testem do wykrywania i ilościowego oznaczania wyizolowanego DNA wirusa CMV z wykorzystaniem technologii real-time PCR. Zasadą działania jest jednoczesna amplifikacja i detekcja określonego obszaru genomu CMV z wykorzystaniem technologii 5’ Taqman.
- Cztery Wzorce Pomiaru Ilościowego zapewniają dokładny pomiar wiremii CMV
- Kontrola Czułości potwierdza skuteczność testu
- Kontrola Wewnętrzna (IC2) sprawdza zarówno wydajności ekstrakcji, włączając etap lizy, jak i obecność potencjalnej obecności inhibitorów.
- Zawiera niezbędne odczynniki do diagnostyki in vitro zoptymalizowane do wykrywania i ilościowego oznaczania CMV
Prosta procedura
Korzystanie z zestawu CMV R-gene® jest proste. Wystarczy dodać wyizolowane DNA do gotowego do użycia premiksu amplifikacyjnego i rozpocząć reakcję na odpowiednim termocyklerze Real-Time zgodnie z opisanym w „Instrukcji Technicznej” programem.
zasada_argene.jpg
BIOMERIEUX, niebieskie logo, ARGENE, R-gene, easyMAG and NucliSENS są używanymi i / lub zastrzeżonymi znakami towarowymi należącymi do bioMérieux, lub jedenego z jego oddziałów, lub jednego z jego spółek. Każda inna nazwa lub znak towarowy jest własnością odpowiedniego właściciela.
| CMV R-gene® (69-003B) | |
|---|---|
| Zasada działania testu | Wykrywanie genomowego DNA i oznaczanie ilościowe miana wirusa CMV |
| Informacje dotyczące składania zamówień | Nr katalogowy 69-003B: CMV R-gene® zestaw ilościowy. Także dostępny pod nr katalogowym 69-003: CMV R-gene® zestaw ilościowy KOMPLETNY (zawiera 69-003B zestaw ilościowy i produkt o numerze katalogowym 67-000 zestaw do izolacji DNA) |
| Technologia | Real-Time PCR / 5‘ nukleaza Taqman |
| Sekwencja wykrywana | gen kodujący białko ppUL83 |
| Rodzaj próbki |
Krew pełna, Płyn mózgowo-rdzeniowy (CSF), Osocze, Surowica, Popłuczyny oskrzelowo-pęcherzykowe (BAL), Mocz, Materiał z biopsji |
| Limit dtekekcji | LoD 95% : 22 kopie/PCR (555 kopie/ml) LoD 5% : 1 kopia/ml (30 kopii/ml) |
| Zakres pomiaru ilościowego | Do 107 copies/ mL |
| Kontrole | Kontrola ekstrakcji + inhibicji, kontrola czułości, kontrola negatywna |
| Czas uzyskania wyników | 75 minut (etap ekstrakcji nie jest uwzględniony) |
| Jednostki | Kopie/ml lub stosując współczynnik konwersji przekształcone do jednostek międzynarodowych IU/ml z wykorzystaniem pierwszego standardu międzynarodowego WHO |
| Liczba reakcji | 90 reakcji |
| Warunki przechowywania | -18°C/-22°C dla nr kat. 69-003B (Zestaw ilościowy) +2°C/+8°C dla nr kat. 67-000 (zestaw do izolacji DNA) |
| Zwalidowane manualne i automatyczne systemy do ekstrakcji | QIAamp DNA Blood Mini kit NucliSENS® easyMAG® MagNA Pure Compact MagNA Pure LC MagNA Pure 96 QIAcube QIAsymphony SP |
| m2000sp VERSANT kPCR Molecular System SP | |
| Zwalidowane platformy do amplifikacji* | Life Technologies (Applied Biosystems) LightCycler RotorGene VERSANT kPCR Molecular System AD Biorad DX Real-Time system Stratagene / Agilent |
| Status | Do diagnostyki in vitro |
Fakty na temat CMV
Czym jest CMV?
Ludzki wirus cytomegalii (HCMV) z rodziny Herpesviridae jest wirusem w otoczce, zbudowanym z dwuniciowego DNA. Po zakażeniu pierwotnym, do którego często dochodzi w dzieciństwie, ludzki wirus CMV w ciele żywiciela przechodzi w okres utajenia. U zdrowych osób zakażenie przebiega najczęściej bezobjawowo, HCMV może powodować nawracające infekcje wtórne, podczas przewlekłej lub przemijającej immunosupresji.
Kto jest najbardziej zagrożony?
Wirus HCMV jest głównym czynnikiem zakaźnym po przeszczepie allogenicznym szpiku kostnego lub przeszczepie narządu. Długotrwała gorączka może być jedynym objawem klinicznym, jednak możliwe jest również wiele powikłań, w tym śródmiąższowe zapalenie płuc. Jest to główne powikłanie, które występuje u około 20% wszystkich biorców i jego nieleczony rozwój jest niebezpieczny (90% śmiertelność). Ponadto zakażenie wirusem HCMV jest czynnikiem powodującym lub przyspieszającym odrzucenie przeszczepu lub GVH (reakcja przeszczep przeciwko gospodarzowi). Dodatkowo pogarsza immunosupresję i sprzyja nadkażeniom.
Przypadki zakażenia wirusem HCMV podczas HIV/AIDS spadły o 80% od momentu rozpoczęcia wysoce aktywnego leczenia antyretrowirusowego, badanie jest nadal ważne, aby zapewnić kontrolę CMV i zapobiec powiązanym infekcjom oportunistycznym. Najczęstszymi objawami klinicznymi u pacjentów z HIV/AIDS są zapalenie siatkówki i wrzody żołądka występującymi podczas głównego etapu immunosupresji (w którym średnia liczba limfocytów T CD4+ wynosi poniżej 50/mm3).
W czasie ciąży pojawienie się pierwotnego zakażenia matczynego powoduje powikłania w 50% przypadków zakażenia płodu, z których 10% stanowią przypadki ciężkie, w szczególności z wystąpieniem upośledzenia funkcji neurologicznych
Jakie są korzyści z molekularnych badań CMV?
Test Real-Time PCR pozwala na do szybkie i specyficzne wykrycie wirusa CMV przed pojawieniem się objawów klinicznych, jest to szczególnie ważne dla pacjentów po przeszczepie (narządów lub szpiku) i pacjentów chorych na AIDS. Badanie pomaga śledzić skuteczność aktywnego leczenia i pozwala monitorować nawroty po leczeniu.
CMV R-gene® i pierwszy międzynarodowy standard CMV (1st WHO International Standard for Human Cytomegalovirus)
Potrzebują Państwo obliczyć swój współczynnik konwersji, aby wyrazić wyniki uzyskane przy pomocy testu CMV R-gene® w IU / ml? Proszę pobrać protokół obliczeń.
| Pobierz Protokół » | Pobierz plik Excel » | Pobierz Plakat » |
Jeśli chcą Państwo zamówić Międzynarodowy Standard WHO CMV (CMV WHO International Standard) (kod 09-162). proszę o kontakt z NIBSC pod podanym adresem:
http://www.nibsc.org/products/biological_reference_materials/product_catalogue/detail_page.aspx?catid=09/162
Uwaga: podane przeliczniki na plakacie są tylko ilustracją do wymienionych kombinacji. bioMérieux zdecydowanie zaleca, aby określić współczynnik konwersji w swoim laboratorium.
CMV R-gene®: PUBLIKACJE
- Cytomegalovirus load in inflamed intestinal tissue is predictive of resistance to immunosuppressive therapy in ulcerative colitis.
Roblin X, Pillet S, Oussalah A, Berthelot P, Del Tedesco E, Phelip JM, Chambonnière ML, Garraud O, Peyrin-Biroulet L, Pozzetto B. Am J Gastroenterol. 2011 Nov;106(11):2001-8. Epub 2011 Jul 26. - Cytomegalovirus infection in severe burn patients monitoring by real-time polymerase chain reaction: A prospective study
Bordes et al. Burns. 2011 May;37(3):434-9. Epub 2011 Jan 14. - Interêt de la recherche du cytomegalovirus par polymerase chain reaction dans le syndrome de Posner-Schlossman
Rodier-Bonifas et al. Journal français d'ophtalmologie, 2011 ; 34, 24-29 - Evaluation of new commercial real-time PCR quantification assay for prenatal diagnosis of cytomegalovirus congenital infection.
Ducroux A, Cherid S, Benachi A, Ville Y, Leruez-Ville M.J Clin Microbiol. 2008 Jun;46(6):2078-80. Epub 2008 Apr 16. - Multicentric evaluation of a new commercial cytomegalovirus (CMV) real-time PCR quantification assay
Gouarin S, Vabret A, Scieux C, Agbalika F, Cherot J, Mengelle C, Deback C, Petitjean J, Dina J, Freymuth F. J Virol Methods. 2007 Dec;146(1-2):147-54. Epub 2007 Jul 27. - Detection of cytomegalovirus (CMV) DNA in EDTA whole-blood samples: evaluation of the quantitative artus CMV LightCycler PCR kit in conjunction with automated sample preparation.
Michelin BD, Hadzisejdic I, Bozic M, Grahovac M, Hess M, Grahovac B, Marth E, Kessler HH. J Clin Microbiol. 2008 Apr;46(4):1241-5. Epub 2008 Feb 13.