CMV HHV6,7,8 R-gene®
Zestaw Real-time PCR do detekcji i pomiaru ilościowego DNA CMV, HHV-6, oraz detekcji DNA HHV-7 i HHV-8
- Dokładny pomiar ilościowy miana wirusa CMV i HHV-6 z szerokim zakresem liniowości
- Detekcja HHV-7 i HHV-8
- Gotowy do użycia zestaw z kontrolą wewnętrzną i kontrolami ilościowymi w zestawie dla CMV i HHV-6
- Test posiada certyfikat CE- IVD dla najpopularniejszych systemów do ekstrakcji oraz platformach real-time PCR
Potrzebujesz więcej informacji
CMV HHV6,7,8 R-gene® zalety
CMV, HHV-6, HHV-7, HHV-8 są odpowiedzialne za szerokie spektrum chorób. Dlatego ważne jest, aby osiągnąć optymalne wykrywanie i monitorowanie infekcji CMV, HHV-6, HHV-7 i HHV-8. CMV HHV6,7,8 R-gene® jest idealnym rozwiązaniem, oferującym szybką i dokładną detekcję.
Możliwość wykrycia zakażenia przed objawami klinicznymi poprawia możliwości zarządzania, badania pacjentów podczas leczenia w celu sprawdzenia jego skuteczności i badania po leczeniu w celu monitorowania nawrotów. Dodatkowo – dla zwiększenia efektywności i kompleksowości - używanie wielu zestawów R-gene® pozwala na wykrywanie różnych wirusów z jednej próbki i analizy różnych próbek dla jednego wirusa w tym samym czasie.
- Czułość i powtarzalność
- Dokładna detekcja CMV i HHV6; identyfikacja infekcji HHV-7, HHV-8
- Szeroki zakres liniowości dla CMV and HHV-6
- Standaryzacja
- Wspólny profil testów - wiele oznaczeń w jednym czasie
- Wspólna procedura postępowania z pozostałymi testami R-gene® (CMV R-gene®, HSV1 HSV2 VZV R-gene®, BK Virus R-gene®, Adenovirus Virus R-gene®, EBV R-gene®, Parvovirus B19 R-gene®)
- Elastyczność
- Zwalidowany dla wielu różnych typów próbek
- Możliwość wykonania manualnej lub automatycznej izolacji próbki z wykorzystaniem takich aparatów jak NucliSENS® easyMAG® oraz przygotowanie reakcji z wykorztaniem takiego systemu jak stacja pipetująca easySTREAM™
- Zatwierdzony dla najpopularniejszych platform real-time PCR
Wszystko co potrzebne w jednym zestawie
Zestaw CMV HHV6,7,8 R-gene® jest gotowym do użycia testem do wykrywania i ilościowego oznaczania wyizolowanego DNA wirusa CMV i HHV6 oraz wykrywania HHV-7 i HHV-8 z wykorzystaniem technologii real-time PCR. Zasadą działania jest jednoczesna amplifikacja i detekcja określonego obszaru genomu CMV, HHV-6, HHV-7 i HHV-8 z wykorzystaniem technologii 5’ Taqman.
- Cztery Wzorce Pomiaru Ilościowego zapewniają dokładny pomiar wiremii CMV i HHV-6
- Kontrola Czułości potwierdza skuteczność testu
- Kontrola Wewnętrzna (IC2) sprawdza zarówno wydajności ekstrakcji, włączając etap lizy, jak i obecność potencjalnej obecności inhibitorów
- Zawiera niezbędne odczynniki do diagnostyki in vitro zoptymalizowane do wykrywania i ilościowego oznaczania CMV (90 reakcji), HHV-6 (30 reakcji) oraz detekcji HHV-7 (10 reakcji), HHV-8 (10 reakcji).
- Dodatkowe odczyniki: możliwość zwiększenia reakcji PCR dzięki HHV6 premix r-gene® (69-100R6 – 60 reakcji), HHV7 premix r-gene® (69-100R7 - 20 reakcji), HHV8 premix r-gene® (69-100R8 - 20 reakcji)
Prosta procedura
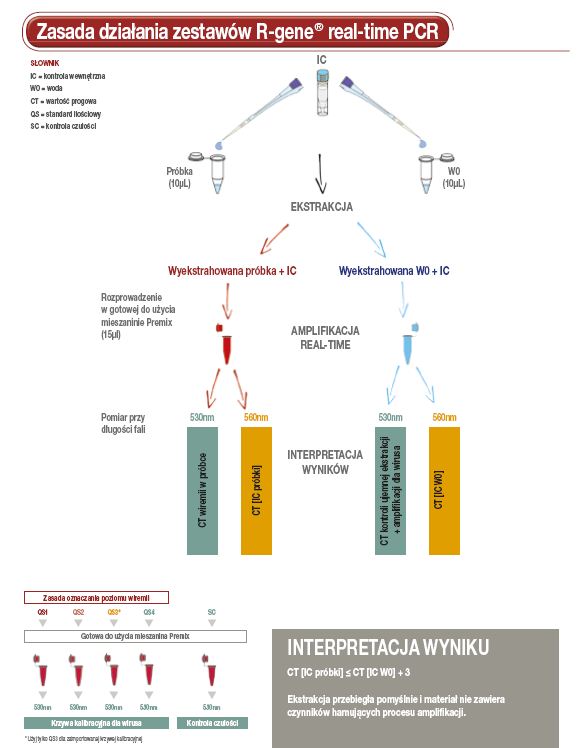
Korzystanie z zestawu the CMV HHV6,7,8 R-gene® jest proste. Wystarczy dodać wyizolowane DNA do gotowego do użycia premiksu amplifikacyjnego i rozpocząć reakcję na odpowiednim termocyklerze Real-Time zgodnie z opisanym w „Instrukcji Technicznej” programem.
zasada_argene.jpg
BIOMERIEUX, niebieskie logo, ARGENE, R-gene, easyMAG and NucliSENS są używanymi i / lub zastrzeżonymi znakami towarowymi należącymi do bioMérieux, lub jedenego z jego oddziałów, lub jednego z jego spółek. Każda inna nazwa lub znak towarowy jest własnością odpowiedniego właściciela.
Żadna inna nazwa lub znak towarowy jest własnością jego odpowiedniego właściciela.
| CMV HHV6,7,8 R-gene® (69-100B) | |
|---|---|
| Zasada testu |
Wykrywanie genomowego i oznaczanie ilościowe DNA wirusa CMV i HHV-6 Wykrywanie genomowego DNA HHV-7 i HHV-8 |
| Informacje dotyczące składania zamówień | Nr katalogowy 69-100B: CMV HHV6,7,8 R-gene® Zestaw do detekcji i oznaczania ilościowego Także dostępny pod nr katalogowym 69-100: CMV HHV6,7,8 R-gene® zewtaw do detekcji i oznaczania ilościowego KOMPLETNY (zawiera 69-100B zewtaw do detekcji i oznaczania ilościowego i produkt o numerze katalogowym 67-000 zestaw do izolacji DNA) Dodatkowe odczynniki: 69-100R6: HHV6 premix r-gene® 69-100R7: HHV7 premix r-gene® 69-100R8: HHV8 premix r-gene® |
| Technologia | Real-Time PCR / 5‘ nuclease nukleaza Taqman |
| Sekwencja wykrywana | CMV: gen kodujący białko ppUL83 HHV-6: U57 gen HHV-7: U42 gen HHV-8: ORF26 gen |
| Rodzaj próbki * | Krew pełna, Płyn mózgowo-rdzeniowy (CSF), Osocze, Surowica, Popłuczyny oskrzelowo-pęcherzykowe (BAL), Mocz, materiał z biopsji |
| Limit dtekekcji | CMV: LoD 95% : 446 Kopii/ ml dla próbki krwi pełnej HHV-6: LoD 95% : 555 Kopii/ml dla próbki krwi pełnej |
| Zakres pomiaru ilościowego | CMV dla próbki krwi pełne: 9.43 log (Cp/ml) do 2.63 log (Cp/ml) CMV w próbce płynu owodniowego: 9.43 log (Cp/ml) do 2.63 log (Cp/ml) |
| Kontrole | Kontrola ekstrakcji + inhibicji, kontrola czułości, kontrola negatywna |
| Czas uzyskania wyników | 75 minut (etap ekstrakcji nie jest uwzględniony) |
| Jednostki | Kopie/ml |
| Liczba reakcji | 140 reakcji |
| Warunki przechowywania | -18°C/-22°C dla nr kat. 69-003B (Zestaw ilościowy) +2°C/+8°C dla nr kat.. 67-000 (zestaw do izolacji DNA) |
| Zwalidowane manualne i automatyczne systemy do ekstrakcji* | QIAamp DNA Blood Mini kit QIAcube NucliSENS® easyMAG® MagNA Pure Compact MagNA Pure LC MagNA Pure 96 m2000sp VERSANT kPCR Molecular System SP QIAsymphony SP |
| Zwalidowane platformy do amplifikacji* | Life Technologies (Applied Biosystems) LightCycler 1.0 LightCycler 2.0 LightCycler 480 System II RotorGene VERSANT kPCR Molecular System AD DX Real-Time system CFX96 Stratagene / Agilent |
| Status | Do diagnostyki in vitro, znak CE w Europie |
* proszę pytać
Fakty na temat CMV, HHV-6, HHV-7 i HHV-8
Informacje na temat CMV, HHV-6, HHV-7, HHV-8?
Cytomegalovirus (CMV), ludzki herpesewirus-6 (HHV-6), ludzki herpesewirus -7 (HHV-7) oraz ludzki herpesewirus -8 (HHV-8) charakteryzują się wysoką seroprewalencją (50% do 100% w zależności od położenia geograficznego). Są wszechobecne i odpowiadają za szeroki zakres chorób u ludzi. Do zakażenia pierwotnego dochodzi często we wczesnym dzieciństwie. Rozsiewanie wirusa w krwi rzadko prowadzi do występowania objawów klinicznych, a w przypadku wystąpienia mają one łagodny charakter.
Kto jest najbardziej zagrożony?
Z wyjątkiem infekcji wrodzonej, powaga infekcji zależy od stanu immunologicznego żywiciela (osobami podatnymi na chorobę są często pacjenci chorzy na AIDS i pacjenci po przeszczepie). Wirus CMV powoduje choroby neurologiczne, pneumopatie, a, w najpoważniejszych przypadkach, jest przyczyną wysokiej śmiertelności u osób ze stanem obniżonej odporności. Wirusy HHV-6 i HHV-7często powodują oportunistyczne infekcje u osób ze stanem obniżonej odporności. Wirusy te mogą najprawdopodobniej stać się przyczyną ostrzejszej wtórnej infekcji CMV w wyniku wzajemnej krzyżowej reaktywacji.Podejrzewa się, że wirus HHV-6 jest odpowiedzialny za mononukleozę, powiększenie węzłów chłonnych oraz zapalenie wątroby w przypadku infekcji pierwotnej u osób dorosłych. Wirus HHV-8 powoduje choroby limfoproliferacyjne, takie jak mięsak Kaposiego, choroba Castlemana i niektóre rodzaje chłoniaka.
Jakie są korzyści z molekularnej diagnostyki wirusów MV, HHV-6, HHV-7, HHV-8?
Zestaw CMV HHV 6,7,8 R-gene® umożliwia wykrywanie i oznaczenie ilościowe genomu wirusów CMV i HHV-6 oraz wykrycie genomu wirusów przed pojawieniem się objawów klinicznych, co jest szczególnie ważne dla pacjentów z obniżoną odpornością. Badanie pomaga śledzić skuteczności aktywnego leczenia i pozwala monitorować nawroty po leczeniu.
CMV HHV6,7,8 R-gene® : PUBLIKACJE
Updated international consensus guidelines on the management of cytomegalovirus in solid-organ transplantation.
Kotton CN, Kumar D, Caliendo AM, Asberg A, Chou S, Danziger-Isakov L, Humar A; Transplantation Society International CMV Consensus Group.
Transplantation. 2013 Aug 27;96(4):333-60
- Cytomegalovirus Load in Infl amed Intestinal Tissue Is Predictive of Resistance to Immunosuppressive Therapy in Ulcerative Colitis
Xavier Roblin, Sylvie Pillet, Abderrahim Oussalah, Philippe Berthelot, Emilie Del Tedesco, Jean-Marc Phellip, Marie-Laure Chambonnière, Olivier Garrau, Laurent Peyrin-Biroulet and Bruno Pozzetto.
Am J Gastroenterol. 2011 Nov;106(11):2001-8 - Intérêt de la recherche du cytomegalovirus par polymerase chain reaction dans le syndrôme de Posner-Schlossman.
C.Rodier-Bonifas, P.-L Cornut, G.Billaud, B.Lina, C.Burillon, P.Denis.
Journal Français d'ophtalmologie 2011 34, 24-29 - Cytomegalovirus infection in severe burn patients monitoring by real-time polymerase chain reaction : A prospective study
J.Bordes, J.Maslin, B.Prunet, E.d'Aranda, G.Lacroix, P.Goutorbe, E.Dantzer, E.Meaudre.
Burms (2011), doi:10.1016/j.burns.2010.11.006. - Detection of Cytomegalovirus DNA in EDTA Whole Blood Samples: Evaluation of the Quantitative artus® CMV LC PCR Kit in Conjuntion with Automated Sample Preparation.
Birgit D.A. Michelin, Ita Hadzisejdic, Michael Bozic, Maja Grahovac, Markus Hess, Blazenka Grahovac, Egon Marth, Harald H. Kessler.
J.Clin. Microbiol., February 2008. - Detection of human herpesviruses HHV-6, HHV-7 and HHV-8 in whole blood by real-time PCR using the new CMV, HHV-6, 7, 8 R-gene kit.
Deback C, Agbalika F, Scieux C, Marcelin AG, Gautheret-Dejean A, Cherot J, Hermet L, Roger O, Agut H.
J Virol Methods. 2008 May;149(2):285-91. Epub 2008 Mar 10. - Detection of Human Herpesviruses HHV-6, HHV-7 and HHV-8 in Whole Blood by Real-Time PCR Using the New CMV, HHV-6, 7, 8 R-gene® kit.
Claire Deback, M.D.; Felix Agbalika; Catherine Scieux; Anne-Geneviève Marcelin; Agnès Gautheret-Dejean; Janine Cherot; Laurence Hermet; Odile Roger; Henri Agut.
J Virol Methods May 2008:149(2):285-91. - Evaluation of New Commercial Real-Time PCR Quantification Assay for Prenatal Diagnosis of Cytomegalovirus Congenital Infection.
Aurélie Ducroux, Samira Cherid, Alexandra Benachi, Yves Ville, and Marianne Leruez-Ville.
J of Clinical Microbiology. June 2008,p.2078-2080. - Monitoring of human Cytomegalovirus infection in immunosupressed patients using real time PCR on whole blood.
C.Deack, A.M Fillet, N. Dehdin, B. Barrou, S. Vamous, F. Najoullah, F. Bricaire, H. Agut.
J. of Clinical Virology 40 (2007) 173-179. - Multicentric evaluation of a new commercial cytomegalovirus real-time PCR quantitation assay.
Gouarin S, Vabret A, Scieux C, Agbalika F, Cherot J, Mengelle C, Deback C, Petitjean J, Dina J, Freymuth F.
J Virol Methods.2007 dec;146(1-2):147-54
Plakaty :
- bioMérieux Argene Range verifications on the ViiA7 (Fast and Standard Blocks) and ABi 7500 Fast Dx Real Time PCR Platforms
Magro Stephane; Delarivière Audrey; Berriot Aurelie; Turc Amelie; Moiroud Elise; Derome Andrew; Alberti-Segui Cristina; Grosz Sophie; Vidal Celine; Poyet-Gelas Fanny and Barranger Come
ESCV 2014, Prague - Comparison of the EZ1 XL advanced and the Magna Pure instruments for the extraction of whole blood before DNA quantification of CMV, EBV, HHV 6 and Adenovirus
Marie Gueudin, Alexandre Louvel, Jean-Christophe Plantier
Laboratoire de virologie, CHU de Rouen, Université de Rouen, France
ECV 2013 - Validation of the combination of the QIAsymphony extractor with the R-gene kits for the quantification of viral DNA loads: application for cytomegalovirus and Epstein Barr virus DNA monitoring in whole blood specimens
Sylvie Pillet et al
Virology Unit, University Hospital of Saint-Etienne
ECV 2013 - Validation Of A New EasyMAG Protocol For Extraction Of Viral DNA From Whole Blood: Application To Cytomegalovirus DNA Load Monitoring
Sylvie Pillet et al
Virology Unit, University Hospital of Saint-Etienne
ECV 2013 - Improvement of NucliSENS® easyMAG® whole blood extraction protocol for virus
Vignoles et al.
CVS 2013 - CMV R-gene™ real time PCR assay and the candidate 1st WHO International Standard for Human Cytomegalovirus : Standardization of nucleic acid amplification techniques
Vignoles et al.
ESCV 2011 - CMV R-gene® real-time PCR assay and the 1st WHO International standard for CMV: Standardization of PCR techniques
Vignoles M. ; Barranger N. ; Bertrand M. ; Raoux N. ; Magro S. ; Barranger C. ; Joannes M.
Poster 14th annual meeting of th eeuropean society for clinical virology, Madeira, 2011 - Evaluation of CMV R-gene PCR (Argene) coupled with EasyMag Biomérieux extraction for CMV viral load quantification in amniotic fluid
Alain et al.
French National reference center for Cytomegaloviruses, CHU Dupuytren, Limoges France
CMV Workshop Nuremberg 2011 - Evaluation of CMV R-gene PCR(Argene) coupled with esayMAG® Biomérieux extraction for CMV viral load quantification in amniotic fluid.
Alain S. ; Boyer B. ; Vignoles M. ; Joannes M. ; Barranger C. ; Ploy M-C.
CMV Workshop Nüremberg 2011.
- Measurement of HSV1, CMV, HHV6 and EBV viral loads in 83 bronchoalveolar lavage (BAL) from lung transplant recipients.
Germi et al.
Unit of Virus Host Cell Interactions, Grenoble
ESCV 2011 - Human herpesvirus 6 infection after hematopoietic stem cell transplantation : prevalence and risk factor. Jeulin et al.
Laboratory of Virology, Nancy University Hospital, France
CVS 2010 - Assessment of cytomegalovirus (cmv) load in hematopoietic stem cell transplant recipients by cmv antigenemia and two different real-time pcr assays
Colak et al.
Akdeniz university, School of Medicine, Antalya.
ESCV 2009 - Surveillance of cytomegalovirus (cmv) and human herpesvirus-6 (hhv6) infections in pediatric allogeneic stem cell transplant récipients
Mutlu et al.
University School of Medicine Medical Microbiology Department, Antalya, Turkey.
ESCV 2009 - HHV6 encephalitis in immunocompetent patients, is it a myth ?
Rozé et al.
Département de Microbiologie, Centre Hospitalier Universitaire de Brest
CVS 2009 - Comparative evaluation of the NucliSENS® easyMAG™ automated system for the extraction of viral DNA from whole blood samples: application to the monitoring of Cytomegalovirus (CMV) and Epstein-Barr virus (EBV) loads
Pillet et al.
Laboratoire de Bacteriologie-Virologie-Hygiène, Hopital Nord, CHU de Saint-Etienne, France.
ECCMID 2008 - Performance Evaluation of the Argene Biosoft CMV HHV-6, 7, 8, R-gene Assay
Zhang et al.
North Shore LIJ Health System Laboratories, Lake Success, NY
CVS 2007